USOS Y APLICACIONES BIOLÓGICAS DE LAS AMIDAS
Las amidas son un tipo de compuestos orgánicos que pueden considerarse derivados de ácidos o aminas. Por ejemplo, la amida alifática simple acetamida (CH3-CO-NH2) está relacionada con el ácido acético en el sentido de que el grupo BOH del ácido acético se sustituye por un grupo -NH2. Recíprocamente, se puede considerar que la acetamida es un derivado del amoniaco por sustitución de un hidrógeno por un grupo acilo. Las amidas se derivan no sólo de los ácidos carboxílicos alifáticos o aromáticos, sino también de otros tipos de ácidos, como los que contienen azufre o fósforo.
El término amidas sustituidas se refiere a las amidas que tienen uno o ambos hidrógenos del nitrógeno reemplazados por otros grupos; por ejemplo, la N,N-dimetilacetamida. Este compuesto puede considerarse también como una amina, la acetildimetilamina. Las amidas son, generalmente, de naturaleza neutra con respecto a su capacidad de reacción en comparación con los ácidos o aminas de los que se derivan y algunas de ellas son ligeramente resistentes a la hidrólisis. Las amidas simples de los ácidos carboxílicos alifáticos (con excepción de la formamida) se encuentran en estado sólido a temperatura ambiente, mientras que las amidas sustituidas de los ácidos carboxílicos alifáticos pueden ser líquidas, con puntos de ebullición relativamente altos. Las amidas de los ácidos carboxílicos aromáticos o sulfónicos son, generalmente, sólidas. Existe una gran variedad de métodos para la síntesis de las amidas.

Las amidas no sustituidas de los ácidos carboxílicos alifáticos se utilizan ampliamente como productos intermedios, estabilizantes, agentes de desmolde para plásticos, películas, surfactantes y fundentes. Las amidas sustituidas, como la dimetilformamida y la dimetilacetamida tienen propiedades disolventes muy poderosas. La dimetilformamida se utiliza principalmente como disolvente en procesos de síntesis orgánica y en la preparación de fibras sintéticas. También constituye un medio selectivo para la extracción de compuestos aromáticos a partir del petróleo crudo y un disolvente para colorantes. Tanto la dimetilformamida como la dimetilacetamida son componentes de disolventes de pinturas. La dimetilacetamida se emplea también como disolvente de plásticos, resinas y gomas y en numerosas reacciones orgánicas.

La acetamida se utiliza para la desnaturalización del alcohol y como disolvente de numerosos compuestos orgánicos, como plastificante y como aditivo para el papel. También se encuentra en lacas, explosivos y fundentes. La formamida es un ablandador de papel y pegamentos y se utiliza como disolvente en la industria de plásticos y farmacéutica.
Algunas amidas alifáticas no saturadas, como la acrilamida, son monómeros reactivos que se utilizan en la síntesis de polímeros. La acrilamida se utiliza también en la síntesis de colorantes, adhesivos, en el engomado del papel y el apresto de textiles, en tejidos plisados y en el tratamiento del agua y las aguas residuales. En la industria del metal se utiliza para el procesado de minerales y en ingeniería civil, para la construcción de cimientos de presas y túneles.
Las poliacrilamidas se utilizan ampliamente como agentes floculantes en el tratamiento del agua y las aguas residuales y como agentes reforzadores en los procesos de fabricación de papel en la industria papelera.
Los compuestos de amidas aromáticas son importantes productos intermedios en la industria de los colorantes y en medicina. Algunos también son repelentes de insectos. Riesgos La gran variedad de estructuras químicas posibles de las amidas se refleja en la diversidad de sus efectos biológicos. Algunas son completamente inocuas, por ejemplo, las amidas de los ácidos grasos simples de cadena larga, como las amidas de los ácidos esteárico u oléico.
Por otra parte, algunos miembros de esta familia han sido clasificados por la Agencia Internacional para la Investigación sobre el Cáncer (IARC) en el Grupo 2A (probable carcinógeno humano) o en el Grupo 2B (posible carcinógeno humano). Con la acrilamida se han observado efectos neurológicos en el hombre y en animales de experimentación. La dimetilformamida y la dimetilacetamida producen lesiones hepáticas en los animales y los efectos teratogénicos de la formamida y la monometilformamida se han demostrado experimentalmente. Si bien existe una gran cantidad de información acerca del metabolismo de algunas amidas, la naturaleza de sus efectos tóxicos aún no se ha explicado a nivel molecular o celular. Muchas amidas simples son, probablemente, hidrolizadas por la acción de amidasas inespecíficas en el hígado y el ácido producido se excreta o se metaboliza a través de los mecanismos normales. Algunas amidas aromáticas, como la N-fenilacetamida (acetanilida), se hidroxilan en el anillo aromático y, seguidamente, se conjugan y se excretan. La capacidad de ciertas amidas de penetrar en el organismo a través de la piel intacta es especialmente importante para la adopción de medidas preventivas.
De igual manera, existen otros medicamentos como la atorvastatina, que es un bloqueador de la producción de colesterol y uno de los medicamentos más vendidos en el mundo desde el 2003, según cifras de la industria farmacéutica Pfizer, y contiene un grupo amido al igual que el Reyataz, un inhibidor de proteasas usado en el tratamiento de VIH. Otro medicamento es el Gleevec (inhibidor de la porteintirosincinasa usado en el tratamiento de la leucemia crónica mieloide) y el Altace (un inhibidor de ACE usado en el tratamiento de la hipertensión y enfermedades del corazón) que también contienen amidas.

PROPIEDADES QUÍMICAS
REACCIONES DE LAS AMIDAS
Conversión de las amidas en ácidos carboxílicos
Hidrólisis ácida: Las amidas experimentan hidrólisis para producir ácidos carboxílicos y amoniaco o una amina mediante el calentamiento en un ácido acuoso o en una base acuosa.
Hidrolisis básica: la hidrólisis básica sucede por la adición nucleofílica del OH- al grupo carbonilo de la amida, seguida por la eliminación del ion amiduro (-NH2) y la desprotonación subsecuente del ácido carboxílico formado inicialmente por el ion amiduro. Los pasos son reversibles, con el equilibrio desplazado hacia el producto por la desprotonación final del ácido carboxílico.
La hidrólisis de amidas en bioquímica
La reacción es catalizada por enzimas proteasas y se efectúa por un mecanismo casi idéntico al de la hidrólisis de grasas. Esto es, una sustitución nucleofílica en el grupo acilo inicial de un grupo alcohol en la enzima en un enlace amida en la proteína da una acil enzima intermediaria que entonces experimenta la hidrólisis.
Reducción de amidas para producción de aminas
El efecto neto de una reacción de reducción de amidas es la conversión del grupo carbonilo de la amida en un grupo metileno (COnCH2). Este tipo de reacción es específica de las amidas y no ocurre con otros derivados de ácidos carboxílicos.
La reacción es efectiva con ambos tipos de amidas, cíclicas y acíclicas, o lactamas, y es un buen método para la preparación de aminas cíclicas.
Preparación de los nitrilos
El método más sencillo de preparación de los nitrilos es la reacción SN2 del CN con un haluro de alquilo primario o secundario. Otro método para la preparación de nitrilos es por la deshidratación de una amida primaria, RCONH2. Con frecuencia se utiliza para la reacción el cloruro de tionilo, aunque también funcionan otros agentes deshidratantes como el POCl3.
Amidas cíclicas- Lactamas
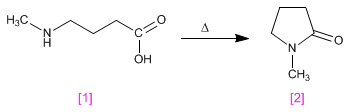
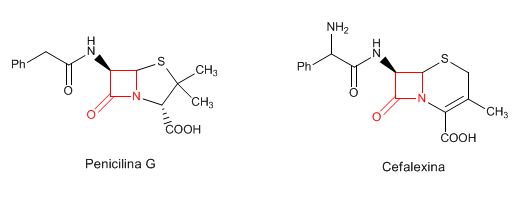
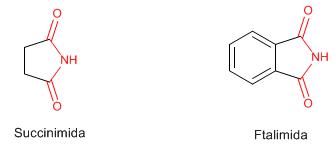
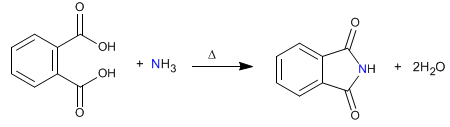
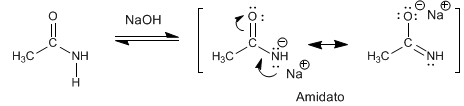
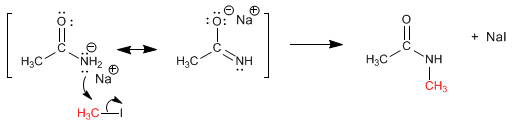
SÍNTESIS DE AMIDAS
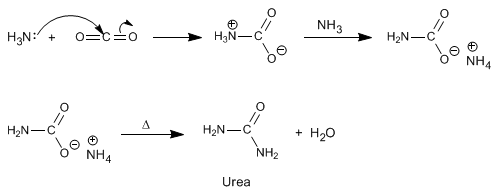
a) Las amidas se pueden obtener por reacción de aminas con haluros de alcanoílo y anhídridos.
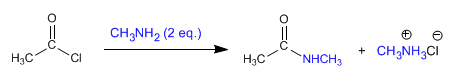
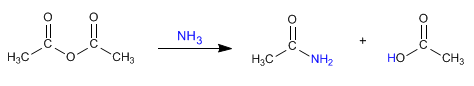
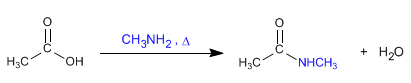
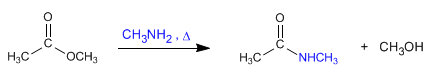
Referencias
AQM. (29 de 06 de 2013). Obtenido de AMIDAS, APLICACIÓN Y
SÍNTESIS: http://www.actaquimicamexicana.uadec.mx/?p=595
Quimica en casa. (03 de 05 de 2016). Obtenido de LAS AMIDAS: BENEFICIOS
Y RIESGOS PARA NUESTRA SALUD:
https://quimicaencasa.com/las-amidas-beneficios-riesgos-nuestra-salud/
AMIDAS, R. D. (15 de 07 de 2017). Obtenido de
http://www.qorganica.es/QOT/T11/reactividad_amidas_exported/index.html
Fernández, G. (s,f). Química Orgánica. Amidas. Obtenido de
https://www.quimicaorganica.org/amidas/480-formacion-de-amidatos.html
Guias de productos
quimicos. (s,f). Obtenido de
PROPIEDADES DE LAS AMIDAS:
https://www.insst.es/documents/94886/162038/3.+Amidas+-+Aminas+alif%C3%A1ticas+-+Formaci%C3%B3n+de+nitrosaminas+-+Aminas+arom%C3%A1ticas
Morrison,
R.; Boyd, R. 1998. Química Orgánica. 5° Edición. PEARSON: Naucalpan de Juárez, Edo. De México, Capítulo 27.
947-950.


No hay comentarios.:
Publicar un comentario